 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有反应NO(g)+CO(g)=N2(g)+CO2(g)=-373.4kJ·mol-1</sup>,欲使有害气体CO和NO取得最高的转化率,则应选择()。
A.低温、高压
B.高温、高压
C.低温、低压
D.高温、低压
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.低温、高压
B.高温、高压
C.低温、低压
D.高温、低压
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“有反应NO(g)+CO(g)=N2(g)+CO2(g)=-3…”相关的问题
更多“有反应NO(g)+CO(g)=N2(g)+CO2(g)=-3…”相关的问题
反应N2(g)+3H2(g)=2NH3(g)(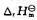 >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压
有如下两组数据:
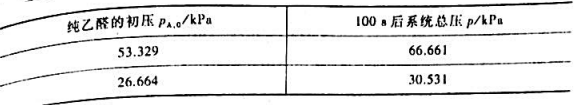
(1)求反应级数n,速率常数kp;
(2)若活化能为190.4kJ·mol-1,问在什么温度下其速率常数k,为518℃下的2倍.
已知298.15K时,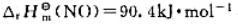 ,反应N2(g)+O2(g)=2NO(g)的
,反应N2(g)+O2(g)=2NO(g)的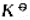 =4.5×10-31。
=4.5×10-31。
(1)计算500K时该反应的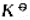 ;
;
(2)汽车内燃机中汽油的燃烧温度可达1575K,根据平衡移动原理说明该温度是否有利于NO的生成。
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为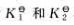 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)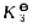 的=()。
的=()。
已知反应CO2(g)+H2(g)=CO(g)+H2O(g)在973K时的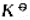 =0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时
=0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时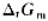 (973K)时值并判断反应进行的方向。
(973K)时值并判断反应进行的方向。
理趣气体反应CO(g)+2H2(g)→CH3OH(g)的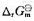 >0与温度T的关系为:
>0与温度T的关系为: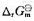 =-21660+52.92T/K>0.若要使反应的平衡常数K0>1.则应控制的反应温度.()
=-21660+52.92T/K>0.若要使反应的平衡常数K0>1.则应控制的反应温度.()
A.必须低于409.3K
B.必须高于409.3K
C.必须等于409.3K
试用热力学数据表计算823K下以下反应的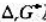 及
及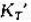 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?
已知NO与H2可进行如下化学反应:
2NO(g)+2H2(g)→N2(g)+2H2O(g)
在一定温度下,某密闭容器中等摩尔比的NO与H2混合物在不同初始压力下的半衰期如下:

求反应的总级数n.