 更多“合成氨反应是()反应”相关的问题
更多“合成氨反应是()反应”相关的问题
第2题
已知复合反应是分为以下两步进行的: 则该复合反应的速率方程为().A、 B、 C、 D、
已知复合反应是分为以下两步进行的: 则该复合反应的速率方程为().A、 B、 C、 D、
点击查看答案
已知复合反应 是分为以下两步进行的:
是分为以下两步进行的:

则该复合反应的速率方程为().
A、
B、
C、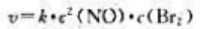
D、
第4题
已知反应的标准摩尔焓变,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措
已知反应 的标准摩尔焓变
的标准摩尔焓变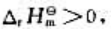 ,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
A、将系统的体积压缩为原来的1/2
B、体积保持不变,加入惰性气体使压力增大到原来的2倍
C、压力保持不变,加入惰性气体使体积增大到原来的2倍
D、体积保持不变,加入NO气体使压力增大到原来的2倍
第5题
化学平衡状态的特征,描述错误的是()。
A.反应是可逆反应或可逆过程
B.正反应和逆反应速率相等
C.平衡时体系中反应物和生成物的浓度将不再改变
D.到达平衡状态,反应速度即为零,反应立即结束
第7题
已知A,B,C和D四个化学反应在298.15K时的标准摩尔焓变分别为100kJ·mol-1,200kJ·mol
-1,-126kJ·mol-1和-50.0kJ·mo-1,标准摩尔熵变分别30.0J·mol-1·K-1,-113J·mol-1·K-1,84.0J·mol-1·K-1和-105J·mol-1·K-1.则在标准状态下,任何温度都能自发进行的反应是();只能在低温下自发进行的反应():任何温度都不能自发进行的反应是():只能在高温下自发进行的反应是()
点击查看答案
第8题
环丁烯异构化反应是一级反应:150℃时,速率常数k=2.0×10-4s-1,气态环丁烯的初始浓
环丁烯异构化反应是一级反应:
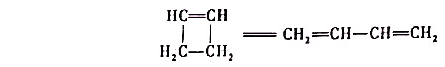
150℃时,速率常数k=2.0×10-4s-1,气态环丁烯的初始浓度为1.89×10-3mol·dm-3,试求:
(1)20min时环丁烯的浓度;
(2)环丁烯的浓度变成1.00×10-3mol·dm-3所需时间。
第10题
反应在某温度下达到平衡。 (1)若其他条件不变,加入催化剂是否会引起平衡移动? (2)若增大任
反应 在某温度下达到平衡。
在某温度下达到平衡。
(1)若其他条件不变,加入催化剂是否会引起平衡移动?
(2)若增大任一反应物或生成物的分压,化学平衡向哪一方向移动?
(3)升高温度时标准平衡常数是否发生变化?化学平衡向哪一方向移动?
(4)缩小容器的体积增大压力时,化学平衡向哪一方向移动?标准平衡常数是否发生变化?
第11题
规模相当于摧毁西伯利亚森林的那一次在地球大气中的陨石爆炸,威力大概相当于 1200万吨级的核爆炸,一个世纪大概出现一次。由复杂的计算机程序控制的高度自动化的核导弹防御系统对于未预料的情况的反应是无法预测的。如果以上关于由一个复杂的计算机程序控制的高度自动化的核导弹防御系统的陈述是正确的,可以最适当地得出以下哪一项结论?()
A.在它建成后的一个世纪内,该系统会做出不适当的反应并可能由于偶然性而引起一场核战争。
B.如果在地球大气层中发生一次大陨石爆炸,该系统将被摧毁。
C.对于该系统来说,不可能将一次大的陨石爆炸和一件核武器的爆炸区分开来。
D.如果该系统的设计者没有考虑到陨石爆炸这种可能性,那么该系统对一次陨石大爆炸将要做出的反应是不确定的。


 如果结果不匹配,请
如果结果不匹配,请 

















