题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
升高温度可以增大反应速率,其主要原因是()。
A.活化分子百分数增大
B.反应的活化能降低
C.反应的摩尔吉布斯自由能减小
D.反应的速率常数减小
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.活化分子百分数增大
B.反应的活化能降低
C.反应的摩尔吉布斯自由能减小
D.反应的速率常数减小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“升高温度可以增大反应速率,其主要原因是()。”相关的问题
更多“升高温度可以增大反应速率,其主要原因是()。”相关的问题
A、增加了分子的碰撞次数
B、增大了活化分子的百分数
C、降低了反应的活化能
D、促使化学平衡正向移动
某化学反应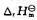 <0,
<0,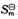 >0,则反应的标准平衡常数()。
>0,则反应的标准平衡常数()。
A.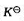 >1且随温度升高而增大
>1且随温度升高而增大
B.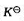 <1且随湿度升高而减小
<1且随湿度升高而减小
C.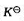 <1且随温度升高而增大
<1且随温度升高而增大
D.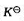 >1且随温度升高而减小
>1且随温度升高而减小
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
某对行反应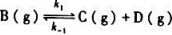 在300K时,k1=10s-1,k-1,=100Pa-1.s-1.当温度升高10°C时k1与k-1均增大一倍,则正、逆反应的活化能
在300K时,k1=10s-1,k-1,=100Pa-1.s-1.当温度升高10°C时k1与k-1均增大一倍,则正、逆反应的活化能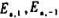 及反应的
及反应的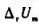 为().
为().
A.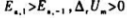
B.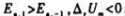
C.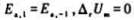
D.