 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
莫尔法测定Cl-时,由于()的溶解度大于()的溶解度,故当用AgNO3标准溶液滴定至化学计量点附近时,才出现()色的()沉淀而指示终点。
莫尔法测定Cl-时,由于()的溶解度大于()的溶解度,故当用AgNO3标准溶液滴定至化学计量点附近时,才出现()色的()沉淀而指示终点。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“莫尔法测定Cl-时,由于()的溶解度大于()的溶解度,故当用…”相关的问题
更多“莫尔法测定Cl-时,由于()的溶解度大于()的溶解度,故当用…”相关的问题
A.用Hg2+盐直接滴定
B.用AgNO3直接滴定
C.用AgNO3沉淀后,返滴定
D.用Pb2+盐沉淀后,返滴定
A.AgI的溶解度太大
B.AgI强烈吸附Ag+
C.Ag2CrO4转化为AgI的速度太慢
D.Ag+离子容易水解
A.本法可测定Cl-,Br-,但不能测定I-,SCN-
B.滴定应在弱酸性介质中进行
C.指示剂K2CrO4的量越少越好
D.莫尔法的选择性较强
A.同离子效益
B.盐效应
C.络合效应
D.无法确定
A.催化反应
B.同离子效应
C.诱导效应
D.盐效应
计算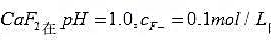 时的溶解度。(已知pKsp(CaF2)=10.57, pKSP(HF)=3.18)
时的溶解度。(已知pKsp(CaF2)=10.57, pKSP(HF)=3.18)
本题通过两个箱中粒子模型的应用实例进行运算:
(1)将KCl晶体放置在金属钾蒸气中加热,K原子受辐射而电离,K→K++e-。K+扩散进入晶体,使晶体的K+离子数目多于Cl-离子数目,晶体的组成变为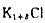 ,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成
,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成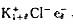 ,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
(2)金属钾的摩尔体积室温时为45.36cm3mol-1,试计算它的Fermi能级(EF),分别以J和eV表示,并和实验测定值2.14eV比较。