 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)试写出下列各电对的电极反应式: ①H+/H2;②O2/H2O;③OH-/H2:④O
(1)试写出下列各电对的电极反应式:
①H+/H2;②O2/H2O;③OH-/H2:④O2/OH-
(2)查表求出①和④的标准电极电势值,并分别写出其电极电势的能斯特方程。
(3)试根据①和④的标准电极电势值及水的离子积常数,求出②和③的标准电极电势值。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)试写出下列各电对的电极反应式:
①H+/H2;②O2/H2O;③OH-/H2:④O2/OH-
(2)查表求出①和④的标准电极电势值,并分别写出其电极电势的能斯特方程。
(3)试根据①和④的标准电极电势值及水的离子积常数,求出②和③的标准电极电势值。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“(1)试写出下列各电对的电极反应式: ①H+/H2;②O2/…”相关的问题
更多“(1)试写出下列各电对的电极反应式: ①H+/H2;②O2/…”相关的问题
试从热力学原理说明直接氯化法从TiO2氯化制取TiCl4的可能性:
TiO2(s)+2Cl2(g)→TiCl4(1)+O2(g)
实际生产过程是在焦炭存在下高温氯化,请写出有关反应式并说明反应的基本原理,计算反应的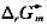 .
.
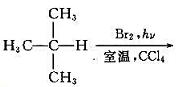
试写出下列各反应生成的一卤代烷,预测所得异构体的比例.
(1)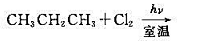
(2)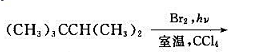
(3)
NO3反应生成白色沉淀,用KMnO4溶液氧化生成丙酸(CH3CH2COOH)和二氧化碳;(B)不与Ag(NH3)2NO3反应,而用KMnO4溶液氧化只生成一种羧酸。试写出(A)和(B)的构造式及各步反应式。
写出异丙醇与下列试制作用的反应式.
(1)Na
(2)AI
(3)冷浓疏酸
(4)H2SO4,>160℃
(5)H2SO4,<140℃
(6)NaBr十H2SO4
(7)红磷+碘
(8)SOCl2
(9)CH3C5H4ASO2Cl
(10)(1)的产物+C2H5Br
(11)(1)的产物+叔丁基氯
(12)(5)的产物+HI(过量)
现有KNO3和NaNO2的混合样品5.000g,制备成500.0mL的溶液,移液25.00mL,用浓度为0.1200mol·L-1的Ce4+标准溶液50.00mL在强酸中氧化,过量的Ce4+用浓度为0.02500mol·L-1的Fe2+标准溶液滴定,用去Fe2+溶液28.40mL,相应的反应如下:
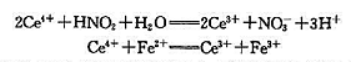
(1)若将第一个反应式作为原电池的电池反应写出该原电池的电极反应并计算该电池反应的ΔrGmθ[已知ϕθ(Ce4++/Ce3+)=1.44V,ϕθ(NO3-/NO2-)=0.934V]
(2)计算试样中NaNO2的质量分数w.[已知M(NaNO2)=69.00g.mol-1]
(3)计算第一步的标准平衡常数Kθ.
解题思路:注意原电池的写法.此题依然是考查电化与热力学、化学平衢间的计算.