 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
称取钢样1.00g,溶解后在500.00mL容量瓶中定容.移取10.00mL,将其中的Mn氧化为MnO42-,
定容为25.00mL.用1.0cm比色皿在520nm处测得吸光度A=0.284,求该钢样中Mn的含量.已知ε(MnO42-)=2.24X103(L·mol-1·cm-1).
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“称取钢样1.00g,溶解后在500.00mL容量瓶中定容.移…”相关的问题
更多“称取钢样1.00g,溶解后在500.00mL容量瓶中定容.移…”相关的问题
(1)实际上所配缓冲溶液的pH为多少?
(2)若要配制pH=0.64三氯乙酸缓冲溶液。需加入多少摩尔强酸或强碱?
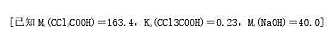
,以磺基水杨酸为指示剂。用0.02000mol·L-1EDTA标准溶液滴定试样中的Fe3+。用去18.16ml.然后将试液调至pH=3.5,加入上述EDTA标准溶液25.0mL,并加热煮沸。再调试液pH=4.5.以PAN为指示剂,趁热用CuSO4标准溶液(每毫升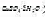 为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
某一原状土样切满于容积为60cm3的环刀内,称得总质量为160.05g(包括环刀质量),取其中25.05g(包括铝盒质量)经105℃烘干至恒重为21.60g(包括铝盒质量),已知环刀质量为 42.40g,铝盒质量为10.96g,试求该土样的天然密度、含水量(小数点后保留两位有效数字)。