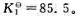题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
单质碘在水中的溶解度很小,但在KI溶液中溶解度显著增大,这是因为()。
A.配位效应
B.离解反应
C.盐效应
D.氧化还原反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.配位效应
B.离解反应
C.盐效应
D.氧化还原反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“单质碘在水中的溶解度很小,但在KI溶液中溶解度显著增大,这是…”相关的问题
更多“单质碘在水中的溶解度很小,但在KI溶液中溶解度显著增大,这是…”相关的问题
碘在水中溶解度很小,但在含有l-的溶液中的溶解度增大,这是因为发生了反应:
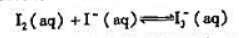
已经测得不同温度下的该反应的标准平衡常数结果见表4-1.

(1)画出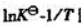 图;
图;
(2)估算该反应的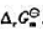 ;
;
(3)计算298K下该反应的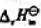 .
.
根据Mg(OH)2的溶度积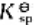 =5.61×10-12,计算:
=5.61×10-12,计算:
(1)Mg(OH)2在纯水中的溶解度。
(2)Mg(OH)2饱和溶液中Mg2+的浓度。
(3)Mg(OH)2在0.01mol·L-1MgCl2溶液中的溶解度。
Mg(OH)2在水中的溶解度为1.12×10-4mol·dm-3,试求其溶解度积常数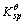 。如果在 0.10dm30.10mol·dm-3MgCl2溶液中加入0.10dm30.10mol·dm-3NH3·Hl2O,试求需加入多少克NH4Cl固体才能够抑制Mg(OH)2沉淀生成。
。如果在 0.10dm30.10mol·dm-3MgCl2溶液中加入0.10dm30.10mol·dm-3NH3·Hl2O,试求需加入多少克NH4Cl固体才能够抑制Mg(OH)2沉淀生成。
试解释以下化学事实:
(1)过渡元素的水合离子多数有颜色,而Se3+,Ti4+,Cu+及Zn2+等水合离子都是无色的.
(2)大多数Cu2+的配离子的空间构型为平面正方形.
(3)HgS可溶于Na2S和NaOH的混合液中,而不溶于(NH4)2S和NH3·H2O的混合液
(4)红色的Cu2O溶于浓氨水中得到溶液是无色的,该溶液在空气中又迅速成为深蓝色溶液.
(5)AgI在溶氨水中不溶,在KCN溶液中立即溶解,滴加Na2S溶液时又产生黑色沉淀.
(6)黄色CdS不能溶于KI溶液中.
(7)硼酸(H3BO3)分子中有三个羟基氢,但硼酸是一元酸.
(8)向硼酸溶液中加人甘油等多羟基化合物后,硼酸就可以用NaOH直接滴定至终点.
(9)化合物K2SiF6,K2SnF6存在,K2SnCl6也存在,但K2SiCl6却不存在.
已知25°C时水的离子积KW=1.008x10-14,NaOH,HCI和NaCl的Amm分别等于0.024811S.m2·mol-1.0.042616S.m2.mol-1和0.012645S.m2.mol-1.
(1)求25°C时纯水的电导率;
(2)利用上述纯水配制AgBr饱和水溶液,测得溶液的电导率k(溶液)=1.664x10-5S.m-1,求AgBr(s)在纯水中的溶解度.
在硝酸钠(NaNO3)的溶解度试验中,测得在不同温度x(℃)下,溶解于100份水中的硝酸钠份数y的数据如下,试求y关于x的线性回归方程.

292K时血红蛋白(Hb)的氧合反应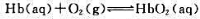
的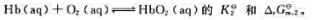 若292K时,空气中p(O2)=20.2kPa,O2在水中的溶解度为2.3×10-4mol·L-1,试求反应
若292K时,空气中p(O2)=20.2kPa,O2在水中的溶解度为2.3×10-4mol·L-1,试求反应