 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
化学反应过程中系统的内能、焓、功和热量与无化学反应的物理过程中的相应量的含义有何不同?化学反应过程中的焓变化能否直接利用各物质的热性质表计算?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“化学反应过程中系统的内能、焓、功和热量与无化学反应的物理过程…”相关的问题
更多“化学反应过程中系统的内能、焓、功和热量与无化学反应的物理过程…”相关的问题
如图所示,1mol氦气,由状态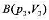 沿直线变到状态 ,求这过程中内能的变化、对外作的功、吸收的热量。
沿直线变到状态 ,求这过程中内能的变化、对外作的功、吸收的热量。

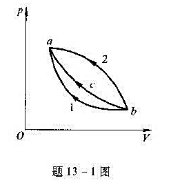
A、b1a过程放热,作负功;b2a过程放热,作负功
B、b1a过程吸热,作负功;b2a过程放热,作负功
C、b1a过程吸热,作正功;b2a过程吸热,作负功
D、b1a过程放热,作正功;b2a过程吸热,作正功
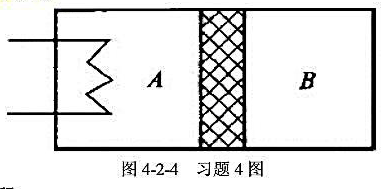
(1)过程中B内气体接受的功量;
(2)过程终了时A、B中气体的温度;
(3)过程中A内气体吸收的热量.
一闭口系统从状态1沿1-2-3途径变化到状态3,传递给外界的热量为52.5 kJ,而系统对外作功为25 kJ,如图所示。 (1)若沿1-4-3途径变化时,系统对外作功15 kJ,求该过程中系统与外界传递的热量。 (2)若系统从状态3沿图示曲线途径到达状态1,外界对系统作功5 kJ,求该过程中系统与外界传递的热量。 (3)若U2=150 kJ,U3=67.5 kJ,求过程2-3传递的热量及状态1的热力学能。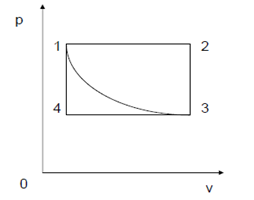
化学反应如下:CH3COOH(g)-CH4+CO2(g),298.15K各物质的数据为

求上述反应在1000K时的标准摩尔反应焓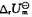 和标准摩尔反应热力学能
和标准摩尔反应热力学能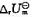 。
。