 更多“某单原子分子理想气体在等压过程中吸热QP=200J。求在此过…”相关的问题
更多“某单原子分子理想气体在等压过程中吸热QP=200J。求在此过…”相关的问题
第1题
OH分子于1964年在星际空间被发现。(1)试按分子轨道理论只用O原子的2p轨道和H原子的1s轨道叠加,写
OH分子于1964年在星际空间被发现。
(1)试按分子轨道理论只用O原子的2p轨道和H原子的1s轨道叠加,写出其电子组态;
(2)在哪个分子轨道中有不成对电子?
(3)此轨道是由O和H的原子轨道叠加形成,还是基本上定域于某个原子上?
(4)已知OH的第一电离能为13.2eV,HF的第一电离能为16.05eV,它们的差值几乎和O原子与F原子的第一电离能(15.8eV和18.6eV)的差值相同,为什么?
(5)写出它的基态光谱项。
第3题
烟台某生产企业出口一批冷冻食品(检验检疫类别为PR/QS),出境口岸为烟台。在办理报检业务过程中,应向检验检疫机构申请的证单不包括()。
A.出境货物通关单
B.出境货物换证凭单
C.动植物检疫许可
D.集装箱检验检疫结果单
第4题
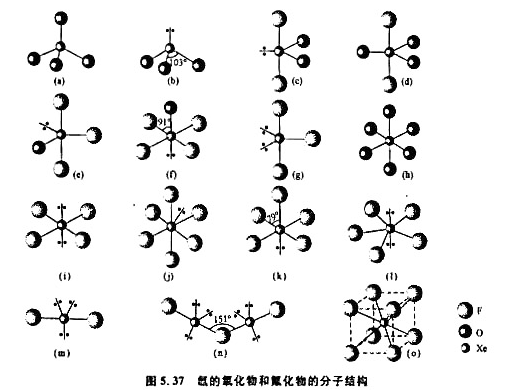
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?
第5题
大连某生产企业出口一批冷冻食品(检验检疫类别为P.R/Q.S),出境口岸为大连。在办理报检业务过程中,应向检验检疫机构申请的证单有()。
A.出境货物通关单
B.集装箱检验检疫结果单
C.出境货物换证凭单
D.动植物检疫许可证
第6题
● 某软件公司正在设计一个图像处理软件,该软件需要支持用户在图像处理过程中的撤销和重做等动作,
为了实现该功能,采用 (54) 最为合适。
点击查看答案
(54)
A. 单例模式
B. 命令模式
C. 访问者模式
D. 适配器模式
第7题
太原某生产企业向法国出口一批瓶装醋,外包装为纸箱,出境口岸为上海。在办理本批货物检验检疫有关手续的过程中,按照取得证单的先后顺序,以下排序的正确的是()
A.出境货物通关单,品质证书,出境货物运输包装性能检验结果单
B.品质证书,出境货物运输包装性能检验结果单,出境货物通关单
C.出境货物运输包装性能检验结果单,品质证书,出境货物通关单
D.出境货物换证凭单,出境货物运输包装性能检验结果单,出境货物通关单
第10题
下列分子和离子中原子的连接顺序如下:(1)F-N-0,(2)N-S-F,(3)H-N-C-N-H,(4)H一N-C-O,(5)H-C-N-0,(
下列分子和离子中原子的连接顺序如下:
(1)F-N-0,(2)N-S-F,(3)H-N-C-N-H,(4)H一N-C-O,
(5)H-C-N-0,(6)S-C-N-CH,(7)S-C-N-SiH3,(8)H-N-N-N,
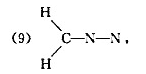
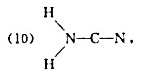
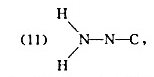
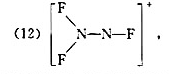
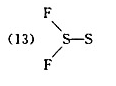
写出它们的结构式,说明分子的几何构型和分子所属的点群。


 如果结果不匹配,请
如果结果不匹配,请 

















