 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
对下列分子和离子CO2,NO2+,NO2,NO2-,SO2,CIO2,O3,等,判断它们的形状,指出中性分子的极性,以及每个分子和离子的不成对电子数。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对下列分子和离子CO2,NO2+,NO2,NO2-,SO2,…”相关的问题
更多“对下列分子和离子CO2,NO2+,NO2,NO2-,SO2,…”相关的问题
将分子或离子:Co(en)33+,NO2+,FHC—C—CHF,(NH2)2CO,C60,丁三烯,B(OH)2,N4(CH2)6。等按下列条件进行归类:
(1)既有极性又有旋光性;
(2)既无极性又无旋光性;
(3)无极性但有旋光性;
(4)有极性但无旋光性。
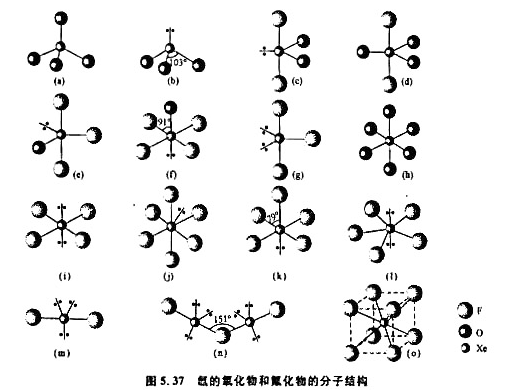
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?
直线形对称构型的I3-离子若成键电子只是5p轨道上的电子(即将5s2电子作为原子实的一部分)。
(1)画出I3-中每个和π轨道的原子轨道叠加图;
(2)面出I2-分子轨道能级图;
(3)试以I原子间的键长(d)和键级(n)关系方程;d=267pm-(85pm)logn,计算I3-中I-I键的键级。实验测定I2分子中I—I键长为267pm,而I3-中I-I键长为292pm。
画出下列分子中孤对电子和键对电子在空间的排布图:
(1)ICl2-,N2O;
(2)H3O+,BrF3,NF3;
(3)ICl4-,IF4+,SbF4-,XeO3F2;
(4)IF3,XeF5+。
写出下列分子的结构式,使其符合十八电子规则:
(1)V2(CO)12;
(2)Ni2(CO)2(C¿214215¿H5)2(羰基成桥);
(3)Cr2(CO)4[C5H5]2;
(4)[Cp3Mo3(CO)5(3-S)]+;
(5)[H5Re3(CO)10]-(有2个Re—Re单键,1个Re Re双键)。
Re双键)。