 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
合成氨反应N2+3H2=2NH3在某温度下建立平衡,达到平衡时,各组分浓度为[N2]=30mo
l·dm-3,[H2]=2.0mol·dm-3,[NH3]=4.0mol·dm-3,求该反应的平衡常数Kc.N2及H2的起始浓度及各自转化率是多少?(设起始时体系中只有氢气和氨气)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“合成氨反应N2+3H2=2NH3在某温度下建立平衡,达到平衡…”相关的问题
更多“合成氨反应N2+3H2=2NH3在某温度下建立平衡,达到平衡…”相关的问题
反应N2(g)+3H2(g)=2NH3(g)(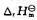 >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压
某温度下,反应 的实验数据如下表所示:
的实验数据如下表所示:
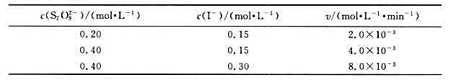
则该反应的速率方程是()。
A、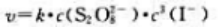
B、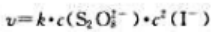
C、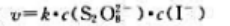
D、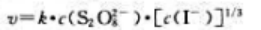
A.在此温度下达到平衡后,两个容器内均有固体物质存在。则下列说法中正确的是()
B.甲容器内的压力大于乙容器内的压力
C.两容器内的压力相等
D.甲容器内的压力小于乙容器内的压力
E.必须进行实验测定才能判断两容器内压力的大小
反应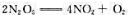 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算:
(1)反应进行了10min后,N2O5分解的百分率;
(2)N2O,分解反应的半衰期。
某温度下,反应
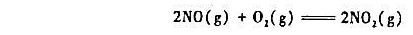
的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2是1级的,当两种反应物浓度都是 0.050mol-1·dm-3时,此反应的反应速率是多少?
某化学反应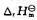 <0,
<0,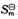 >0,则反应的标准平衡常数()。
>0,则反应的标准平衡常数()。
A.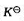 >1且随温度升高而增大
>1且随温度升高而增大
B.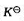 <1且随湿度升高而减小
<1且随湿度升高而减小
C.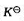 <1且随温度升高而增大
<1且随温度升高而增大
D.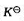 >1且随温度升高而减小
>1且随温度升高而减小
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?