 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试画出下列同核双原子分子的分子轨道图,写出电子构型,计算键级,指出何者最稳定,何者不稳定,且
判断哪些具有顺磁性,哪些具有反磁性.
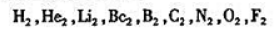
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
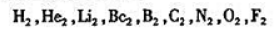
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试画出下列同核双原子分子的分子轨道图,写出电子构型,计算键级…”相关的问题
更多“试画出下列同核双原子分子的分子轨道图,写出电子构型,计算键级…”相关的问题
OH分子于1964年在星际空间被发现。
(1)试按分子轨道理论只用O原子的2p轨道和H原子的1s轨道叠加,写出其电子组态;
(2)在哪个分子轨道中有不成对电子?
(3)此轨道是由O和H的原子轨道叠加形成,还是基本上定域于某个原子上?
(4)已知OH的第一电离能为13.2eV,HF的第一电离能为16.05eV,它们的差值几乎和O原子与F原子的第一电离能(15.8eV和18.6eV)的差值相同,为什么?
(5)写出它的基态光谱项。
直线形对称构型的I3-离子若成键电子只是5p轨道上的电子(即将5s2电子作为原子实的一部分)。
(1)画出I3-中每个和π轨道的原子轨道叠加图;
(2)面出I2-分子轨道能级图;
(3)试以I原子间的键长(d)和键级(n)关系方程;d=267pm-(85pm)logn,计算I3-中I-I键的键级。实验测定I2分子中I—I键长为267pm,而I3-中I-I键长为292pm。
画出下列分子中孤对电子和键对电子在空间的排布图:
(1)ICl2-,N2O;
(2)H3O+,BrF3,NF3;
(3)ICl4-,IF4+,SbF4-,XeO3F2;
(4)IF3,XeF5+。
图a为一量值随时间减小,方向垂直纸面向内的变化电场,均匀分布在圆柱形区域内,试在图b中画出:
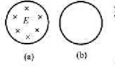
(1)位移电流的大致分布和方向;
(2)磁场的大致分布和方向。