 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
乙醛(A)蒸气的热分解反应为CH2CHO(g)→CH4(g)+co(g).518℃下在一恒容容器中的压力变化
乙醛(A)蒸气的热分解反应为CH2CHO(g)→CH4(g)+co(g).518℃下在一恒容容器中的压力变化
有如下两组数据:
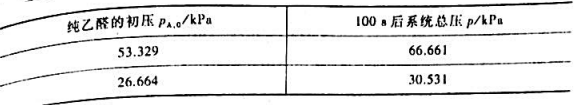
(1)求反应级数n,速率常数kp;
(2)若活化能为190.4kJ·mol-1,问在什么温度下其速率常数k,为518℃下的2倍.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有如下两组数据:

(1)求反应级数n,速率常数kp;
(2)若活化能为190.4kJ·mol-1,问在什么温度下其速率常数k,为518℃下的2倍.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“乙醛(A)蒸气的热分解反应为CH2CHO(g)→CH4(g)…”相关的问题
更多“乙醛(A)蒸气的热分解反应为CH2CHO(g)→CH4(g)…”相关的问题
NOCI分解反应为2NOCI→2NO+Cl2实验测得NOCI的浓度与时间的关系如下:
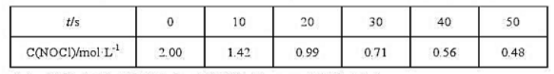
求各时间段内反应的平均速率:用作图法求t=25s时的瞬时速率。
A.放热反应;
B.吸热反应;
C.既不放热也不吸热;
D.这两个温度下的平衡常数相等
A.“湿法炼铜”的化学原理可以表示为Fe+CuSO4===FeSO4+Cu
B.电解氯化镁可以制备金属镁,该反应为分解反应
C.工业上用一氧化碳还原氧化铁制备铁,该反应属于置换反应
D.金矿中的金是以单质形式存在,用物理方法可以制得
A.243.6kJ/h?m
B.243.6kW/h?m
C. 220.2kJ/h?m
D. 220.2kW/h?m
按照下图所示的项目工作分解结构,其中空白处的内容应为(38 ).
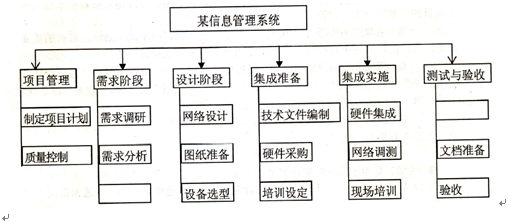
A.需求开发、系统测试
B.需求开发、系统交付
C.需求确认、系统测试
D.需求确认、系统交付
将氧化还原反应 设计成原电池.该原电池的正极反应为().负极反应为()
设计成原电池.该原电池的正极反应为().负极反应为()
反应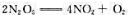 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算:
(1)反应进行了10min后,N2O5分解的百分率;
(2)N2O,分解反应的半衰期。