 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
25℃时,向AgCl饱和溶液中滴加浓HCl溶液,溶液中Ag+浓度下降为1.8×10-8mol·L-1,此时
A.1.0
B.2.0
C.3.0
D.7.0
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1.0
B.2.0
C.3.0
D.7.0
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃时,向AgCl饱和溶液中滴加浓HCl溶液,溶液中Ag+…”相关的问题
更多“25℃时,向AgCl饱和溶液中滴加浓HCl溶液,溶液中Ag+…”相关的问题
试用溶度积规则解释下列现象:
①CaC¿131132¿O4,可溶于HCl溶液中,但不溶于醋酸溶液中。
②AgCl不溶于稀HCl溶液,但可以溶于氨水,
③CuS沉淀不溶于盐酸但可溶于热的HNO3溶液中。
④往Mg2+的溶液中滴加NH3·H2O产生白色沉淀,再滴加NH4Cl溶液,白色沉淀消失。
A.异黄酮
B.黄酮醇
C.花色素
D.黄酮类
在原电池(一)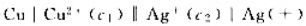 中.若增加CuSO4溶液浓度,则该原电池电动势将();若只在AgNO3溶液中滴加少量NaCl溶液,则原电池电动势将()。(填“不变”,“增大”或“减小”)
中.若增加CuSO4溶液浓度,则该原电池电动势将();若只在AgNO3溶液中滴加少量NaCl溶液,则原电池电动势将()。(填“不变”,“增大”或“减小”)
A.外国投资者的投资比例低于25%的外商投资企业
B.境内内资企业发行B股转化的外商投资股份有限公司
C.向中西部地区再投资设立的外资比例低于25%的企业
D.外商投资企业向中西部以外地区再投资设立的企业
A.在海上遭遇海盗袭击受损
B.在收货人仓库中因火灾受损
C.在海上遇台风和暴雨淋湿受损
D.在卸货时从吊杆上脱落坠地受损
已知M(NH3)42+的 为2.0、5.0、7.0、10.0; M(OH)42+的
为2.0、5.0、7.0、10.0; M(OH)42+的 为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?
为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?