 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池,电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是()①每消耗1mol CH4,可以向外电路提供约 8mol 的电②负极上CH4失去电子,电极反应式为: CH4-8e-+10OH—=CO32-+7H2O③负极上是O2获得电子,电极反应式为O2+2H2O+4e-=4OH-④电池放电后,溶液pH不断升高
A.①②
B.①③
C.①④
D.③④
 答案
答案
A、①②
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成…”相关的问题
更多“有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成…”相关的问题
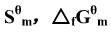 ,数据,求上述反应在25℃时的
,数据,求上述反应在25℃时的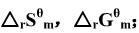
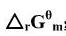 ;
;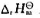 及
及 假定反应中的各气体都可视作理想气体。
假定反应中的各气体都可视作理想气体。
















