 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
今有0°C,40.530kPa的N2气体,分别用理想气体状态方程及vanderWaals方程计算其摩尔体积。实验值为70.2cm3·mol-1.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“今有0°C,40.530kPa的N2气体,分别用理想气体状态…”相关的问题
更多“今有0°C,40.530kPa的N2气体,分别用理想气体状态…”相关的问题
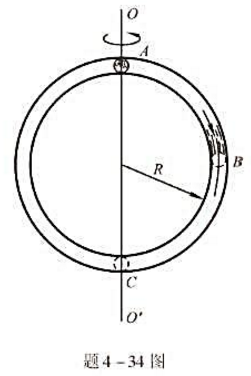
反应N2(g)+3H2(g)=2NH3(g)( >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压
A.987654321
B.4321098765
C.5678901234
D.987651234
A.*p=*q;
B.p=q;
C.*p=&n1;
D.p=*q;
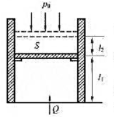
(1)气缸中的气体经历的是什么过程?
(2)气缸中的气体在整个过程中吸了多少热量?
H2,N2与100g水在40℃时处于平衡、平衡总用为105.4kPa.平衡气体经干燥后的体积分数 =0.40.假设溶液的水蒸气压等于纯水的饱和蒸气压,即40℃时的7.33WPa.已知40℃时H2,N2在水中的宁利系数分别为7.61Gpa及10.5GPa,求40℃时水中能溶解H2,N2的质量.
=0.40.假设溶液的水蒸气压等于纯水的饱和蒸气压,即40℃时的7.33WPa.已知40℃时H2,N2在水中的宁利系数分别为7.61Gpa及10.5GPa,求40℃时水中能溶解H2,N2的质量.
A.O(2n)
B.O(n+log2n)
C.O(nlog2n)
D.O(n2)