 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
柠檬酸为三元弱酸,用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。A、
柠檬酸为三元弱酸,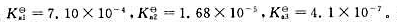 用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
A、1个
B、2个
C、3个
D、无突跃
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
柠檬酸为三元弱酸,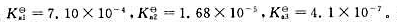 用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
用NaOH标准溶液滴定0.1000mol·L-1柠檬酸溶液时,产生的滴定突跃为()。
A、1个
B、2个
C、3个
D、无突跃
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“柠檬酸为三元弱酸,用NaOH标准溶液滴定0.1000mol·…”相关的问题
更多“柠檬酸为三元弱酸,用NaOH标准溶液滴定0.1000mol·…”相关的问题
为下列(1)~(4)滴定选择合适的指示剂:
(1)用HCl标准溶液滴定乙醇胺溶液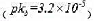 ,指示剂为______.
,指示剂为______.
(2)以邻苯二甲酸氢钾基准物标定NaOH溶液,指示剂为_______.
(3)用佛尔哈德法测定氯离子,指示剂为_______.
(4)用EDTA溶液滴定锌离子,指示剂为_______ .
(填:酚酞、甲基红、铬黑T、铬酸钾、铁铵矾)
A.NH4Cl(Kb(NH3)=1.8×10-5)
B.H2SO4
C.HAc(Ka=1.8×10-5)
D.HCOOH(Ka=1.8×10-4)
A.增加平行测定次数
B.对照试验
C.空白试验
D.设法读准每一次读数
,以磺基水杨酸为指示剂。用0.02000mol·L-1EDTA标准溶液滴定试样中的Fe3+。用去18.16ml.然后将试液调至pH=3.5,加入上述EDTA标准溶液25.0mL,并加热煮沸。再调试液pH=4.5.以PAN为指示剂,趁热用CuSO4标准溶液(每毫升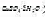 为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
含H2SO4(Mr=98.07)和H3PO4(Mr=98.00)的混合液两份(体积均为25.00mL),分别用0.1018mol·L-1的NaOH标准溶液滴定。第一份以甲基橙(pKHn=3.4)作指示剂,需25.18mL 滴至终点;第二份以酚酞(pKHn=9.1)作指示剂,需35.22mL到达终点。试求混合液中每种酸的浓度?(已知H3PO4的Ka1=10-2.12,Ka2=10-7.21,Ka3=10-12.7)
(已知CaO的摩尔质量58.06gmol1)