 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[判断题]
根据溶度积规则,只要是降低溶液中,有关离子的浓度,沉淀就会溶解。降低离子浓度的方法包括:促使反生成弱电解质、气体或者发生氧化还原反应。()
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“根据溶度积规则,只要是降低溶液中,有关离子的浓度,沉淀就会溶…”相关的问题
更多“根据溶度积规则,只要是降低溶液中,有关离子的浓度,沉淀就会溶…”相关的问题
试用溶度积规则解释下列现象:
①CaC¿131132¿O4,可溶于HCl溶液中,但不溶于醋酸溶液中。
②AgCl不溶于稀HCl溶液,但可以溶于氨水,
③CuS沉淀不溶于盐酸但可溶于热的HNO3溶液中。
④往Mg2+的溶液中滴加NH3·H2O产生白色沉淀,再滴加NH4Cl溶液,白色沉淀消失。
根据Mg(OH)2的溶度积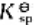 =5.61×10-12,计算:
=5.61×10-12,计算:
(1)Mg(OH)2在纯水中的溶解度。
(2)Mg(OH)2饱和溶液中Mg2+的浓度。
(3)Mg(OH)2在0.01mol·L-1MgCl2溶液中的溶解度。
已知25℃时AgCl(s);水溶液中Ag+,CI-的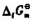 分别为-109.789kJ·mol-1,
分别为-109.789kJ·mol-1,
77.107kJ·mol-1和-131.228kJ·mol-1.求25℃下AgCl(s)在水溶液的标准溶度积Kθ及溶解度s.
已知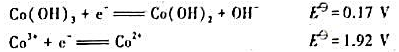
若用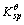 (1)表示Co(OH)3的溶度积常数,
(1)表示Co(OH)3的溶度积常数,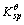 (2)表示Co(OH)2的溶度积常数,试求
(2)表示Co(OH)2的溶度积常数,试求 (1)/
(1)/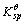 (2)的值。
(2)的值。