 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298.15K时,φθ(MnO2/Mn)=1.224V,φθ(Cl2/CI-)=1.358V,用MnO2和盐
298.15K时,φθ(MnO2/Mn)=1.224V,φθ(Cl2/CI-)=1.358V,用MnO2和盐
酸反应制取Cl2:MnO2(s)+4HCl=Cl2(g)+MnCl2+2H2O.
(1)在标准状态时,能否制取Cl2?
(2)当Mn2+浓度为1.00mol·L-1,Cl2的分压为100kPa时,HCl的浓度至少达到多大时,方可制取Cl2?用计算说明.
(3)按上述反应组成原电池,写出原电池符号.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“298.15K时,φθ(MnO2/Mn)=1.224V,φθ…”相关的问题
更多“298.15K时,φθ(MnO2/Mn)=1.224V,φθ…”相关的问题
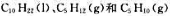 的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应
的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应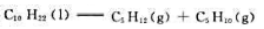 的标准摩尔焓变。
的标准摩尔焓变。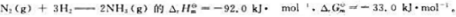 则
则
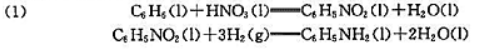
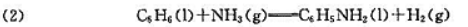
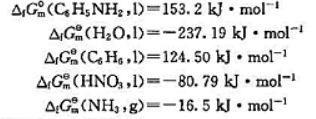

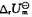 和标准摩尔反应热力学能
和标准摩尔反应热力学能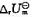 。
。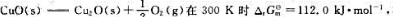 在400K时
在400K时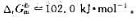
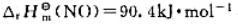 ,反应N2(g)+O2(g)=2NO(g)的
,反应N2(g)+O2(g)=2NO(g)的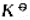 =4.5×10-31。
=4.5×10-31。
















