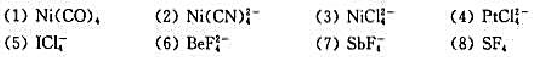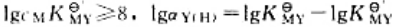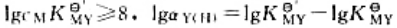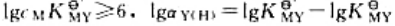更多“配离子的不同几何构型,是由中心离子采用不同类型的杂化轨道与配…”相关的问题
更多“配离子的不同几何构型,是由中心离子采用不同类型的杂化轨道与配…”相关的问题
下列各个配位离子分别具有八面体(六配位)和四面体(四配位)构型,由它们组成的配合物哪些能给出顺磁共振信号。
(1)[Fe(H2O6)]2+;
(2)[Fe(CN)6]6-;
(3)[Fe(CN)6]3-;
(4)[CoF6]3-;
(5)[Co(en)3]3+;
(6)[C(N02)6]4-;
(7)[FeCl4]-;
(8)[Ag(NH3)4]+;
(9)[ZnCl4]2-。
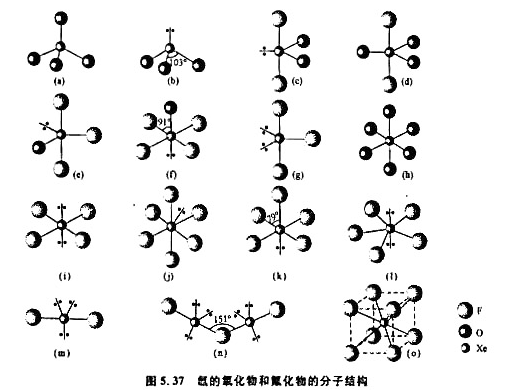
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?
下列分子和离子中原子的连接顺序如下:
(1)F-N-0,(2)N-S-F,(3)H-N-C-N-H,(4)H一N-C-O,
(5)H-C-N-0,(6)S-C-N-CH,(7)S-C-N-SiH3,(8)H-N-N-N,
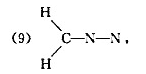
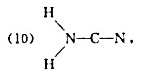
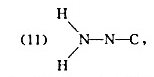
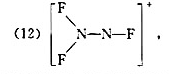
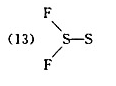
写出它们的结构式,说明分子的几何构型和分子所属的点群。
直线形对称构型的I3-离子若成键电子只是5p轨道上的电子(即将5s2电子作为原子实的一部分)。
(1)画出I3-中每个和π轨道的原子轨道叠加图;
(2)面出I2-分子轨道能级图;
(3)试以I原子间的键长(d)和键级(n)关系方程;d=267pm-(85pm)logn,计算I3-中I-I键的键级。实验测定I2分子中I—I键长为267pm,而I3-中I-I键长为292pm。
本题通过两个箱中粒子模型的应用实例进行运算:
(1)将KCl晶体放置在金属钾蒸气中加热,K原子受辐射而电离,K→K++e-。K+扩散进入晶体,使晶体的K+离子数目多于Cl-离子数目,晶体的组成变为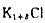 ,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成
,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成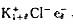 ,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
(2)金属钾的摩尔体积室温时为45.36cm3mol-1,试计算它的Fermi能级(EF),分别以J和eV表示,并和实验测定值2.14eV比较。


 如果结果不匹配,请
如果结果不匹配,请