 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列化学方程式书写正确的是()
A.H2O2H2O+O2↑
B.NaCO3+2HCl=====2NaCl+H2O+CO2↑
C.4Fe+3O2↑Fe3O4
D.NaOH+HCl=====NaCl+H2O
 答案
答案
D、NaOH+HCl=====NaCl+H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.H2O2H2O+O2↑
B.NaCO3+2HCl=====2NaCl+H2O+CO2↑
C.4Fe+3O2↑Fe3O4
D.NaOH+HCl=====NaCl+H2O
 答案
答案
D、NaOH+HCl=====NaCl+H2O
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列化学方程式书写正确的是()”相关的问题
更多“下列化学方程式书写正确的是()”相关的问题
A. CO+Fe2O3===Fe+CO2
B. Hg+H2SO4(稀)===HgSO4+H2↑
C. NaCI+KNO3===NaNO3+KCI
D. FeCI3+3NaOH===Fe(OH)3↓+3NaCI
钛(Ti)被称为继铁、铝之后的第三金属,四川攀枝花和西昌地区的钒钛磁铁矿储量十分丰富。如以下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。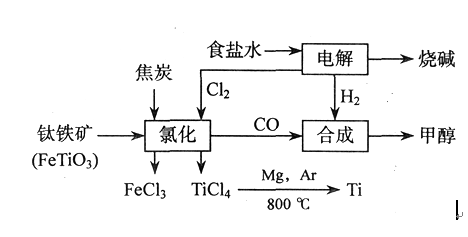 请填写以下空白:
请填写以下空白:
问题一、电解食盐水时,总反应的离子方程式是()。
问题二、写出钛铁矿经氯化法得到四氯化钛的化学方程式:()。
问题三、已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=-641kJ/mol ②Ti(s)+2Cl2(g)=TiCl4(s);△H=-770kJ/mol。以下说法正确的选项是()。
AMg的燃烧热为641kJ/mol
BTi的能量一定比TiCl4高
C等质量的Mg(s)、Ti(s)与足量的氯气反应,前者放出的热量多
D该冶炼Ti法对环境友好
问题四、在上述产业链中,合成192t甲醇理论上需额外补充H2()t(不考虑生产过程中物质的任何损失)。
问题五、以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是()。
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: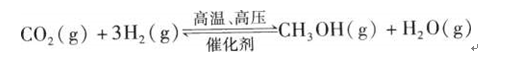
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
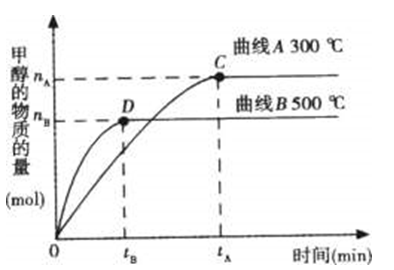
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
A.氨的吹脱的原理化学方程式是
B.氨化和硝化两个过程构成了生物脱氮原理
C.聚磷菌在好氧条件下竞争能力很强
D.污水中的磷的去除只能通过混凝沉淀去除
A.KMnO4+FeSO4+H2SO4―→K2SO4+MnSO4+Fe2(SO4)3+H2O。下列说法正确的是
B.Fe2+的还原性强于Mn2+
C.MnO4-是氧化剂,Fe3+是还原产物
D.生成1 mol水时,转移1.25 mol电子
E.取反应后的溶液加KSCN溶液,可观察到有血红色沉淀生成
A.(V1/V2)3=H1/H2
B.(V1/V2)2=H1/H2
C.V1/V2=H1/H2
D.V1/V2=(H1/H2)2
试写出下列反应的化学方程式,并叙述实验现象:
(1)单质碘溶于在碘化钾溶液中;
(2)在碘化钾溶液中不断通入氯气,直至过量;
(3)少量硫粉与氯酸钾混合均匀后慢慢研磨;
(4)在硝酸汞溶液中逐滴加人碘化钾,直至过量;
(5)高碘酸在酸性条件下与二价锰离子反应;
(6)向次氯酸钠溶液中加入几滴硫酸锰。