 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
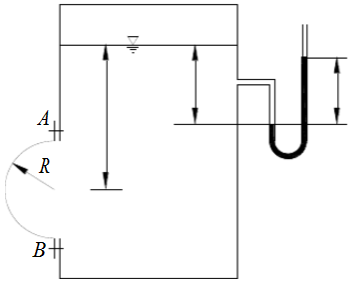
如图所示密闭盛水容器。已知:h1=60cm,h2=100cm,水银测压计读值△h=25cm。试求半径R=0.5m的半球盖AB所受总压力
如图所示密闭盛水容器。已知:h1=60cm,h2=100cm,水银测压计读值△h=25cm。试求半径R=0.5m的半球盖AB所受总压力的水平分力与铅垂分力(水银密度ρHg=13600kg/m3)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
如图所示密闭盛水容器。已知:h1=60cm,h2=100cm,水银测压计读值△h=25cm。试求半径R=0.5m的半球盖AB所受总压力的水平分力与铅垂分力(水银密度ρHg=13600kg/m3)。

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“如图所示密闭盛水容器。已知:h1=60cm,h2=100cm…”相关的问题
更多“如图所示密闭盛水容器。已知:h1=60cm,h2=100cm…”相关的问题
(1)容器内的水面压强p0;
(2)敞口管与容器内的水面高差H;
(3)以真空压强表示poV.
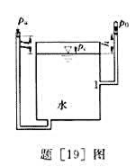
,h2=0.6m,不计能量损失,试求A点流速uA和B点流速uB。水的密度ρ=1000kg/m3。
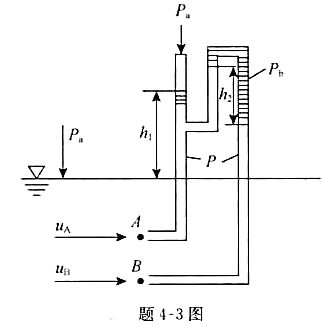
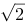 d1 ,d1 管段流体流动的速度头为0.8m水柱,h1 =0.7m,忽略流经AB段的能量损失,按理想流体处理,则()。
d1 ,d1 管段流体流动的速度头为0.8m水柱,h1 =0.7m,忽略流经AB段的能量损失,按理想流体处理,则()。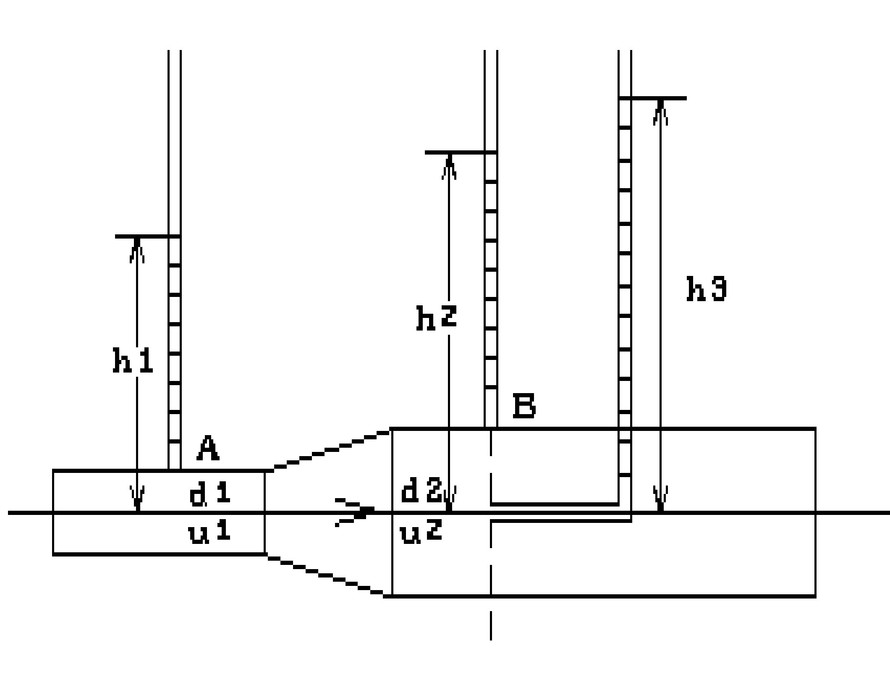
A.h2 = 1.1 m ,h3 = 1.5 m
B.h2 = 0.7 m ,h3 = 0.9 m
C.h2 = 0.7 m ,h3 =0.9 m
D.h2 = 1.3 m ,h3 = 1.5 m
工业上以氨气为原料制备硝酸的过程如下: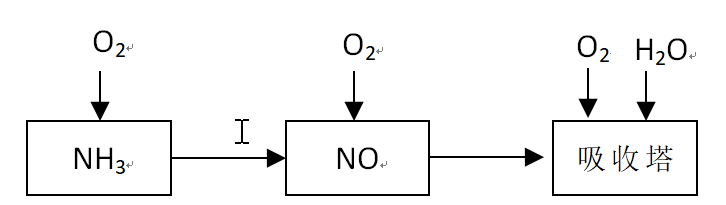 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。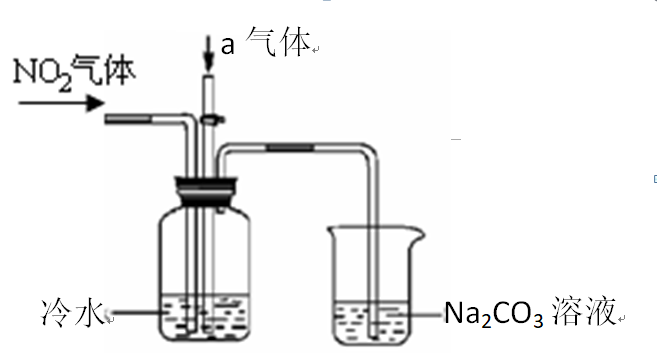
问题一、工业上用氨气制取NO的化学方程式是()。
问题二、连接好该装置后,首先进行的操作是()。
问题三、通入a气体的目的是()。
问题四、盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学反应方程式是2NO2+Na2CO3==NaNO2+()+()
问题五、已知:温度低于21.15℃时,NO2几乎全部转变为N2O4.工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是()。
问题六、一定条件下,某密闭容器中N2O4和NO2的混合气体到达平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
已知某信号m(t)的频谱M(f)如图所示。将它通过传输函数为H1(f)的滤波器后再进行理想抽样。
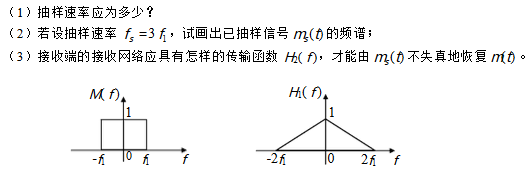
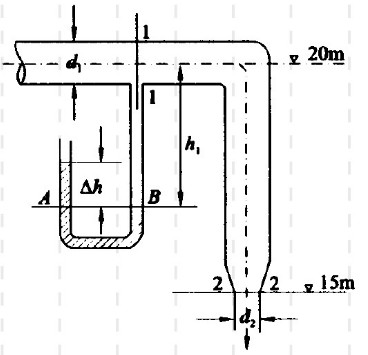
水流通过如图所示的管路,已知U形测压管水银柱高差△h=0.2m,图中h1=0.72m,管径d1=0.1m,管嘴出口直径d2=0.05m,忽略管中的水头损失,试计算管中的流量Q。
已知100°C水的饱和蒸气压为101.325kPa,此条件下水的摩尔蒸发焓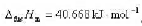 在置于100°C恒温槽中的容积为100dm3的密闭容器中,有压力120kPa的过饱和蒸气。此状态为亚稳态。今过饱和蒸气失稳,部分凝结成液态水达到热力学稳定的平衡态。求过程的Q,ΔU,ΔH,ΔS,ΔA及ΔG。
在置于100°C恒温槽中的容积为100dm3的密闭容器中,有压力120kPa的过饱和蒸气。此状态为亚稳态。今过饱和蒸气失稳,部分凝结成液态水达到热力学稳定的平衡态。求过程的Q,ΔU,ΔH,ΔS,ΔA及ΔG。