 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
下列电池测得E=-0.285V,计算CrO42-的浓度(忽略液接电位).已知Ksp(Ag2CrO
下列电池测得E=-0.285V,计算CrO42-的浓度(忽略液接电位).已知Ksp(Ag2CrO
下列电池
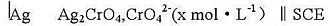
测得E=-0.285V,计算CrO42-的浓度(忽略液接电位).已知Ksp(Ag2CrO4)=9.0X10-12
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列电池
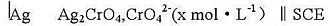
测得E=-0.285V,计算CrO42-的浓度(忽略液接电位).已知Ksp(Ag2CrO4)=9.0X10-12
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列电池测得E=-0.285V,计算CrO42-的浓度(忽略…”相关的问题
更多“下列电池测得E=-0.285V,计算CrO42-的浓度(忽略…”相关的问题
用下列电池按直接电位法测定草酸根离子浓度。
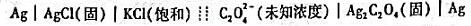
(1)推导出pC2O4与电池电动势之间的关系式
(2)若将一未知浓度的草酸钠溶液置入此电池,在25℃时测得电池电动势为0.402V,Ag-AgCl电极为负极,计算未知溶液的pC2O4。(已知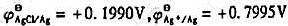 )
)
电池:(一)玻璃电极丨H+(a=?)饱和汞电极(),在25℃时,对pH等于4.00的缓冲溶液,测得电池的电动势为0.209V,当缓冲液由未知液代替时,测得电池的电动势为0.088V,计算未知液的pH.
有如下两个电池:
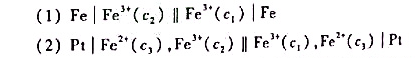
测得其电动势分别为E(1)和E(2),试求E(1)与E(2)之比。
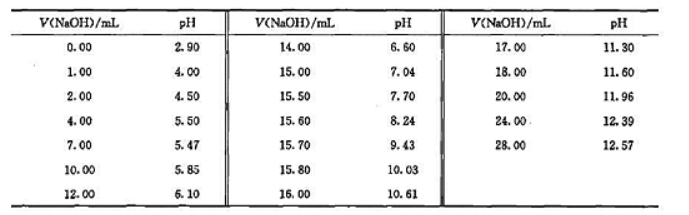
(1)绘制pH-V(NaOH)的曲线,从曲线的拐点确定测定终点.
(2)绘制ΔpH-V(NaOH)的曲线,从曲线的最高点确定测定终点.
(3)用二次微商计算法,从曲线的最高点确定滴定终点.
(4)根据(3)的值计算HCI的浓度.
根据下列反应组成电池
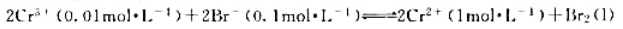
(1)写出电池符号;
(2)计算298K时的电动势,并判断反应自发进行的方向;
已知
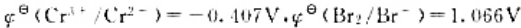
用氟离子选择性电极与Ag/AgC1电极组成测量电池

取25.00mL水样加入25.00mL总离子强度调节液得溶液A,测得其电池电动势为-325mV,若在A溶液中加入1mL1.00X10-3mo1/L溶液,测得电池电动势为-31TmV,若将A溶液用总离子强度调节液稀释一倍,测得电动势为-342mV,求水样中含氟的浓度为多少?